很多时候我们的细胞需要移动。移动细胞指导我们的身体形成(胚胎发育)。免疫细胞漫游以捕获不想要的入侵者。愈合细胞(成纤维细胞)迁移到修补伤口。但并非所有运动都是可取的:当癌细胞获得遍布全身的运动能力(转移)时,肿瘤最危险。某些细菌和病毒可以利用细胞的运动机制侵入我们的身体。了解细胞如何移动 - 以及驱动该过程的棒状肌动蛋白丝 - 是学习如何停止或促进运动以改善人类健康的关键。
现在,使用世界上最强大的显微镜之一,Sanford Burnham Prebys医学发现研究所(SBP)和北卡罗来纳大学教堂山分校(UNC-Chapel Hill)的科学家发现了一种致密,动态和无组织的肌动蛋白丝纳米支架 - - 类似大海捞针 - 是响应分子信号而诱发的。这是研究人员首次在分子水平上直观地观察到一种响应细胞信号而触发的结构 - 这一重要发现扩展了我们对细胞如何运动的理解。这项研究结果发表在国家科学学院院刊美利坚合众国(的PNAS)。
“细胞电子显微镜正在彻底改变我们对细胞内部运作的理解,”该论文的高级作者,SBP生物信息学和结构生物学项目教授Dorit Hanein博士说。“这项技术使我们能够收集细胞区域的强大3D图像 - 类似于MRI,可以创建我们身体的详细图像。我们能够在自然状态下可视化细胞,从而揭示了前所未有的肌动蛋白纳米 - 细胞内的构架。“
在这项研究中,科学家们使用SBP的低温电子显微镜(Titan Krios),人工智能(AI)和量身定制的计算和细胞成像方法来比较小鼠成纤维细胞的纳米级图像和荧光Rac1(一种蛋白质)的时间标记光图像。调节细胞运动,对力或应变(机械传感)和病原体入侵的反应。这种技术复杂的工作流程 - 规模达到五个数量级(数十微米到几纳米) - 需要数年才能发展到目前的稳健性和准确性水平,并且通过结构生物学家团队的实验和计算工作成为可能。 SBP和UNC-Chapel Hill的生物传感器团队。
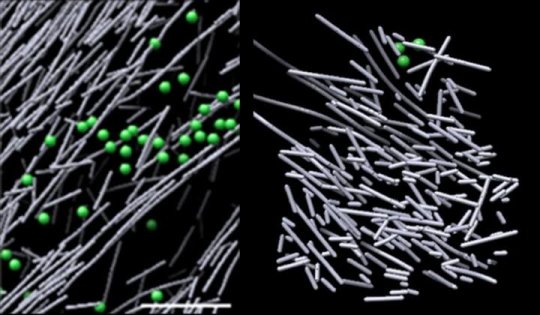
图像显示了由短肌动蛋白杆组成的密集,无组织,类似支架的结构。这些结构在Rac1被激活的特定区域中出现,并在Rac1信号停止时迅速消散 - 仅需2.5分钟。这种动态支架与低Rac1激活区域中的各种其他肌动蛋白组件形成鲜明对比 - 一些由肌动蛋白长而对齐的棒组成,另一些由长肌动蛋白丝两侧分支的短肌动蛋白棒组成。包裹肌动蛋白支架的体积缺乏常见的细胞结构,例如核糖体,微管,囊泡等,可能是由于结构的密度很大。
“我们感到惊讶的是,实验后的实验揭示了这些与Rac1活化相关的区域中未对齐,密集的肌动蛋白棒的独特热点,”Niels Volkmann博士说,他是该论文的共同通讯作者,领导计算部分这项研究,以及SBP生物信息学和结构生物学项目的教授。“我们认为这种疾病实际上是支架的强弱 - 它可以提供灵活性和多功能性,以建立更大,更复杂的肌动蛋白丝结构,以响应其他局部空间线索。”
接下来,科学家们希望扩展该协议,以便可视化更多为响应其他分子信号而创建的结构,并进一步开发该技术以允许进入细胞的其他区域。
“这项研究只是一个开始。现在我们开发了这种定量纳米级工作流程,将动态信号传导行为与电子冷冻断层扫描的纳米级分辨率相关联,我们和其他科学家可以实施这种强大的分析工具,不仅可以破译内部工作原理。细胞运动,但也用于阐明在不受干扰的细胞环境中许多其他大分子机器的动力学,“Hanein说。
她补充道,“肌动蛋白是一种结构蛋白;它与超过150种肌动蛋白结合蛋白相互作用,产生多种结构,每种结构都具有独特的功能。我们有多余的不同信号,我们想要绘制,甚至可以产生更多关于细胞如何移动的见解。“














